CMV Screening - Step 1
26.03.25 - Korrektur Schreibfehler Absatz: Serolog Diagn. Primärinfektion. JKO
21.01.25 - Bei neg IgG/IgM neu Kontrolle IgG/IgM bis 16+0 max. nach ECCI-Empfehlungen. JKO
19.06.23 - Tip zum Verordnen Avidität eingefügt, JKO
30.04.23 - Immer noch Version 1, layout, JKO
30.04.23 - CMV Step 1, 1. Version, frei zugänglich, nur layout, JKO
30.04.23 - Erste Version, frei zugänglich, JKO
- Zweck, Prinzip
- Primäre Prävention
- Serologische Diagnose einer Primärinfektion
- Prinzipien Screening
- Aufklärungsinhalte
- Pitfalls Interpretation
- Serologie Step 1 / Basis
- Interpretation Serologie Step 1 / Basis
- Serologie Step 2
- Kosten
- Literatur
Zweck, Prinzip
Dieser obsgyn-wiki-Eintrag regelt das Vorgehen zur CMV-Serologie im 1. Trimester im Rahmen der Schwangerschaftsvorsorge an der FKL
Auftrag gemäss Expertenbrief No 73 der SGGG: «Alle Frauen sollten so früh wie möglich, idealerweise noch vor Eintreten einer Schwangerschaft, über die Risiken einer CMV-Infektion während der Schwangerschaft und über die Möglichkeit, den CMV-Serostatus zu bestimmen, informiert werden. Dies gilt insbesondere für Frauen mit erhöhtem Expositionsrisiko.»
Das bedeutet: KEIN generelles Screening. Jedoch Aufklärung und Angebot an alle Schwangere.
Primäre Prävention
Der beste Schutz vor einer CMV-Primoinfektion in der Schwangerschaft sind allgemeine Hygienemassnahmen, über die die Schwangere (im LUKIS dokumentiert) aufgeklärt werden müssen.
Hygieneempfehlungen
- obligater Inhalt der Schwangerenberatung im 1. Trimenon
- abzugeben unabhängig vom mütterlichen Serostatus, da eine stattgefundene CMV-Infektion keinen 100%igen Schutz des Kindes bietet
- Besprechung auch praekonzeptionell bei Kinderwunsch
Serologische Diagnose einer Primärinfektion
- Nachgewiesene Serokonversion von IgG oder
- Kombination aus IgM pos, IgG pos, tiefer Avidität
- unklare Befundlage: Besprechung mit Fetomaternalmediziner
Erweiterte Kriterien aus der S2k-Leitlinie der AWMF
- Nachweis einer CMV-IgG-Serokonversion. Dies erfordert idealerweise die Verfügbarkeit von sequentiell abgenommenen Blutproben, wovon die initiale Probe CMV-IgG negativ sein muss. Liegt eine archivierte Serumprobe aus der Vorphase vor, so sollte diese für den Nachweis der Serokonversion eingesetzt werden.
- Nachweis von niederem CMV-IgG, nieder-avidem CMV-IgG in Kombination mit positivem CMV-IgM-Werten oder erhöhten CMV-IgM Indices (Sample/cut-off Index > 1,0). Um Fehlinterpretationen auszuschließen, sollte jeder positive Nachweis einer CMV-Primärinfektion in der Schwangerschaft mit niederem CMV-IgG, niederer CMV-IgG Avidität und IgM-Nachweis im Ligandenassay durch ein Immunblot-Verfahren bestätigt werden.
- Fehlender Nachweis von Antikörpern gegen das CMV-Glykoprotein B (Anti-gB2-IgG mittels Immunblot) in Kombination mit nieder-avidem CMV-IgG und/oder hoch positivem CMV-IgM
(Anm.: Glykoprotein-B («Spätprotein») beschreibt eine Untereinheit der CMV-Antigene, gegen welche bei sehr frischer Infektion noch keine IgG vorhanden sind)
Prinzipien Screening
- Jede im Haus betreute Schwangere wird so früh als möglich = bei erster Schwangerschaftskontrolle oder bei erster Kontrolle an der FKL bis 16 SSW über die Option eines CMV-Screenings aufgeklärt.
- Aufklärung mündlich, im LUKIS in Notiz dokumentiert.
- Insbesondere wichtig bei Risikogruppen:
- Mütter von Kleinkindern (Ein Kleinkind daheim zu haben ist der grösste Risikofaktor für CMV!)
- Immunsupprimierte Schwangere
- Arbeit mit Kindern (Krippen, Gesundheitsambulatorien)
- Zeitpunkt: Frühschwangerschaft / im 1. Trimester, nicht später als 16. SSW
- Bei Verzicht auf Screening: jede an der FKL betreute Schwangere soll bei Erstkontakt bis zum Ende des 1. Trimesters eine Serothek angelegt bekommen (Verordnung „Serothek“ in LUKIS). Zweck: im Falle einer späteren auffälligen Serologie kann auf einen Verlauf zurückgegriffen werden.
- In jedem Zweifelsfall wird nach einer intern oder extern vorliegenden Serothek oder nach einem historischen CMV-Befund gefahndet!
- Bei unklarer Serologie: Im Zweifel wie CMV-Primoinfekt behandeln!
Aufklärungsinhalte
- CMV für Mütter im Normalfall ungefährlich, eine Erstinfektion der Mutter in früher Schwangerschaft mit vertikaler Transmission kann aber selten eine kindliche Erkrankung bewirken
- Ca. 50% der Schwangeren in der Schweiz dürften IgG-positiv sein.
- Bei seropositiver Mutter existiert nur eine sehr geringe Wahrscheinlichkeit einer kindlichen Erkrankung (per Reaktivierung oder Reinfektion).
- In 75% laufen die Erstinfektionen asymptomatisch ab, allfällige Symptome sind nicht spezifisch.
- Nutzen einer CMV-Serologie in der Frühschwangerschaft
- kann eine frische oder kürzlich abgelaufene Primärinfektion erkennen
- in dieser Situation gibt es eine Therapieoption, welche das kindliche outcome verbessern kann
- Problematik einer CMV-Serologie in der Frühschwangerschaft
- es gibt einen niedrigen Anteil unklarer Befunde (IgM pos. in ca. 3% der Fälle)
- falsch positive und falsch negative Befunde sind möglich.
- weitere Diagnostik (Serologie / PCR) kann notwendig werden, bis klar ist, ob es sich um eine Primärinfektion handelt
- bei den Therapieoptionen handelt es sich nicht um Standardtherapien, sondern um Therapieansätze, die auf Studien mit niedriger Fallzahl beruhen – auch wenn die Ergebnisse teils sehr ermutigend sind
Pitfalls Interpretation
- Verglichen werden sollten nur Befunde von Serologien, die sequenziell im gleichen Labor durchgeführt wurden (kein Vergleich Serologie von Labor A mit Serologie von Labor B)
- Es ist unklar, ob die Avidität per Blot oder per Immunoassay besser bestimmbar ist
- IgM ist wenig sensitiv, ist auch bei unspezifischen Reaktionen erhöht
- IgM hat eine mögliche monatelange Persistenz nach Primoinfektion oder ist erhöht bei Reaktivierung einer latenten CMV.
- Negatives IgM schliesst eine Primoinfektion nicht ganz sicher aus.
- Der prognostische Wert einer hohen IgG Avidität vermindert sich mit zunehmendem Schwangerschaftsalter.
- Primoinfektionen zeigen in seltenen Fällen einen raschen Anstieg der Avidität bzw. eine rasche Negativierung von IgM und können somit verpasst werden.
- Sehr niedrige bzw. grenzwertige IgG-Spiegel können zu einer falsch hohen Avidität führen.
- 6% der Primoinfektionen zeigen: IgG pos, IgM pos., hohe IgG-Avidität. Daher zusätzlicher diagnostischer Gewinn per Blot und Markerprofil möglich.
- Cave Markerprofil: auch bei länger zurückliegender CMV-Infektion ist bei 18% der seropositiven Individuen anti-gB-IgG nicht nachweisbar.
Merke: Dieser Eintrag ist nur eine Interpretationshilfe.
Mit Fetomaternalmediziner = Hintergrund Ultraschall sind obligat zu besprechen:
- alle positiven IgMs
- alle unklaren Befunde
Serologie Step 1 / Basis
CMV IgG und IgM, Bestimmung im Labor LUKS
Reminder:
- Falls keine Serologie gewünscht wird: Serologie anlegen
- Wenn (nur wenn!) Avidität gebraucht wird: im LUKIS Nachverordnen, Probe für Nachbestellung anklicken, im Freitextfeld "Welche Probe - Kommentar" eingeben "Avidität aus Probe vom xx.xx.xx")
Interpretation Serologie Step 1 / Basis
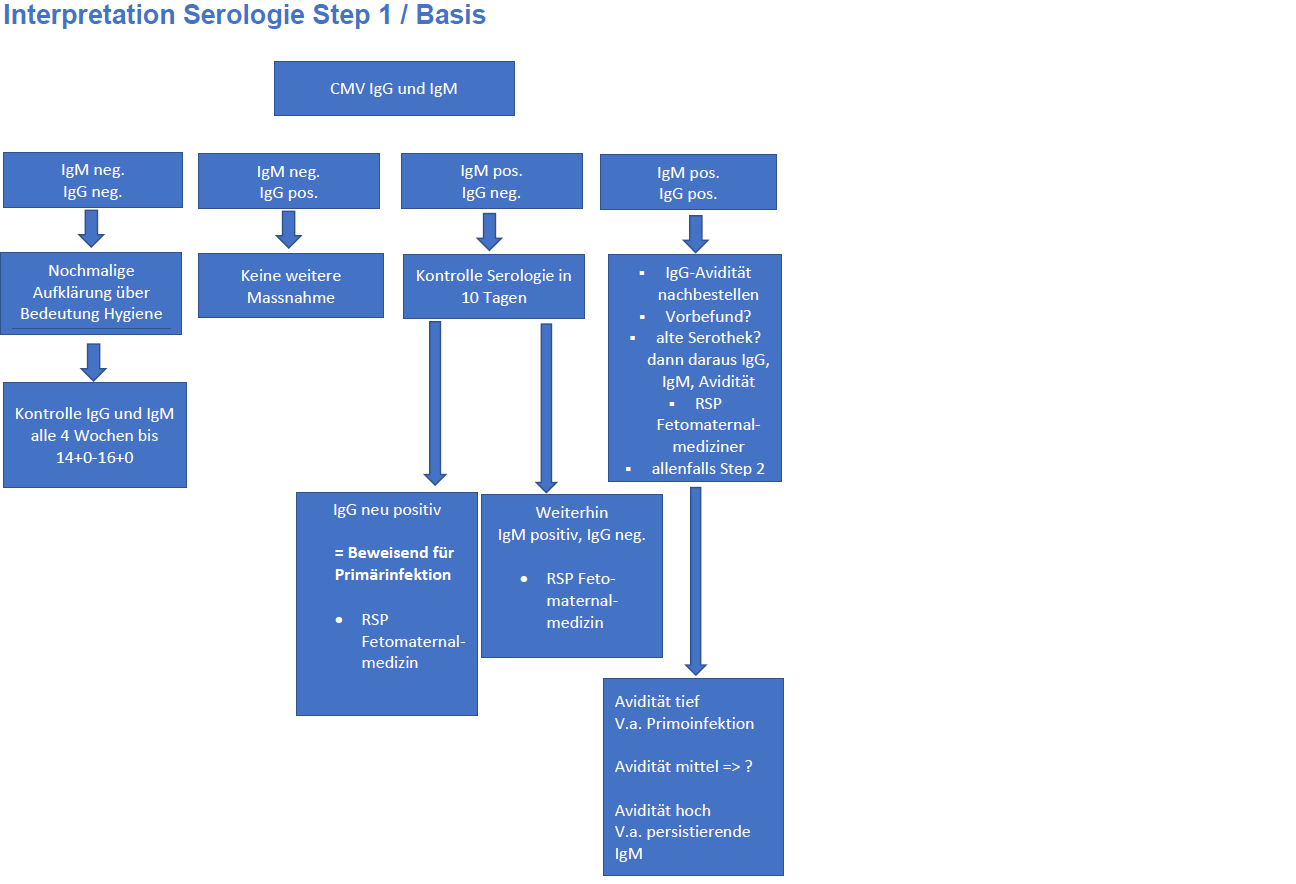
Serologie Step 2
- Optional bei IgG pos und IgM pos. und/oder unklarer Befundlage
- Nur nach RSP Fetomaternalmediziner und im Einzelfall
- Bestimmung von CMV-IgG, -IgM und IgG-Avidität mit Alternativverfahren
=> Link obsgyn-wiki.ch CMV-Screening Step 2
Anm.: wegen der spezifischen Auswertung im geschützten Bereich
Kosten
Step 1
CMV IgG 13.7 und IgM 22.5 TP = 50 TP = total ca. 36.20, Auftragstaxe 24 TP
= Total 60.20 CHF
Literatur
- Expertenbrief der SGGG No 73 (ersetzt No 47)
- AWMF Leitlinie «Labordiagnostik schwangerschaftsrelevanter Virusinfektionen», S2k-Leitlinie, AWMF-Registernummer 093/001
- Arav-Boger R. Strain Variation and Disease Severity in Congenital Cytomegalovirus Infection: In Search of a Viral Marker. Infect Dis Clin North Am. 2015 Sep;29(3):401-14. doi: 10.1016/j.idc.2015.05.009. Epub 2015 Jul 4. PMID: 26154664; PMCID: PMC4552582.
- L. Schäffer, CMV-Screening - Zeit zum Umdenken? info@gynäkologie, 05/2021
- Hyde TB, Schmid DS, Cannon MJ. Cytomegalovirus seroconversion rates and risk factors: implications for congenital CMV. Rev Med Virol. 2010 Sep;20(5):311-26. doi: 10.1002/rmv.659. PMID: 20645278.
- Leruez-Ville M, Magny JF, Couderc S, Pichon C, Parodi M, Bussières L, Guilleminot T, Ghout I, Ville Y. Risk Factors for Congenital Cytomegalovirus Infection Following Primary and Nonprimary Maternal Infection: A Prospective Neonatal Screening Study Using Polymerase Chain Reaction in Saliva. Clin Infect Dis. 2017 Aug 1;65(3):398-404. doi: 10.1093/cid/cix337. PMID: 28419213.
- Leruez-Ville M, Guilleminot T, Stirnemann J, Salomon LJ, Spaggiari E, Faure-Bardon V, Magny JF, Ville Y. Quantifying the Burden of Congenital Cytomegalovirus Infection With Long-term Sequelae in Subsequent Pregnancies of Women Seronegative at Their First Pregnancy. Clin Infect Dis. 2020 Oct 23;71(7):1598-1603. doi: 10.1093/cid/ciz1067. PMID: 31665306.
- Leruez-Ville M, Chatzakis C, Lilleri D, Blazquez-Gamero D, Alarcon A, Bourgon N, Foulon I, Fourgeaud J, Gonce A, Jones CE, Klapper P, Krom A, Lazzarotto T, Lyall H, Paixao P, Papaevangelou V, Puchhammer E, Sourvinos G, Vallely P, Ville Y, Vossen A. Consensus recommendation for prenatal, neonatal and postnatal management of congenital cytomegalovirus infection from the European congenital infection initiative (ECCI). Lancet Reg Health Eur. 2024 Apr 1;40:100892. doi: 10.1016/j.lanepe.2024.100892.
- Chatzakis, C., et al. (2020). "Timing of primary maternal cytomegalovirus infection and rates of vertical transmission and fetal consequences." American Journal of Obstetrics & Gynecology 223(6): 870-883.e811.
- Faure-Bardon, V., et al. (2019). "Sequelae of Congenital Cytomegalovirus Following Maternal Primary Infections Are Limited to Those Acquired in the First Trimester of Pregnancy." Clinical Infectious Diseases 69(9): 1526-1532.
- Enders G, Daiminger A, Bäder U, Exler S, Schimpf Y, Enders M. The value of CMV IgG avidity and immunoblot for timing the onset of primary CMV infection in pregnancy. J Clin Virol. 2013 Feb;56(2):102-7. doi: 10.1016/j.jcv.2012.09.015. Epub 2012 Nov 13. PMID: 23153820.
- Enders M, Daiminger A, Exler S, Ertan K, Enders G, Bald R. Prenatal diagnosis of congenital cytomegalovirus infection in 115 cases: a 5 years' single center experience. Prenat Diagn. 2017 Apr;37(4):389-398. doi: 10.1002/pd.5025. Epub 2017 Mar 16. PMID: 28207161.
- Elkan Miller, T., et al. (2021). "Congenital Cytomegalovirus Infection Following Second and Third Trimester Maternal Infection Is Associated With Mild Childhood Adverse Outcome Not Predicted by Prenatal Imaging." Journal of the Pediatric Infectious Diseases Society 10(5): 562-568.
- Sipewa, M. J., et al. (2002). "Evaluation of a cytomegalovirus glycoprotein B recombinant enzyme immunoassay to discriminate between a recent and a past infection." Journal of clinical microbiology 40(10): 3689-3693.
- Picone et al. Detailed in utero ultrasound description of 30 cases of congenital cytomegalovirus infection. Prenatal Diagnosis. 2014
- Khalil A, et al. ISUOG practice Guidelines: role of ultrasound in congenital infection. Ultrasound Obstet Gynecol, 2020.
- Revello, M. G., et al. (2015). "Prevention of Primary Cytomegalovirus Infection in Pregnancy." EBioMedicine 2(9): 1205-1210.
- Vauloup-Fellous, C., et al. (2009). "Does hygiene counseling have an impact on the rate of CMV primary infection during pregnancy?: Results of a 3-year prospective study in a French hospital." Journal of Clinical Virology 46: S49-S53.
- SAMW; Medizin-ethische Richtlinien: Abgrenzung von Standardtherapie und experimenteller Therapie im Einzelfall. 2015
- Leruez-Ville, M., et al. (2016). "In utero treatment of congenital cytomegalovirus infection with valacyclovir in a multicenter, open-label, phase II study." American Journal of Obstetrics & Gynecology 215(4): 462.e461-462.e410.
- Shahar-Nissan, K., et al. (2020). "Valaciclovir to prevent vertical transmission of cytomegalovirus after maternal primary infection during pregnancy: a randomised, double-blind, placebo-controlled trial." The Lancet 396(10253): 779-785.
- Kagan, K. O., et al. (2019). "Prevention of maternal–fetal transmission of cytomegalovirus after primary maternal infection in the first trimester by biweekly hyperimmunoglobulin administration." Ultrasound in Obstetrics & Gynecology 53(3): 383-389.
- Devlieger R, Buxmann H, Nigro G, Enders M, Jückstock J, Siklós P, Wartenberg-Demand A, Schüttrumpf J, Schütze J, Rippel N, Herbold M, Niemann G, Friese K. Serial Monitoring and Hyperimmunoglobulin versus Standard of Care to Prevent Congenital Cytomegalovirus Infection: A Phase III Randomized Trial. Fetal Diagn Ther. 2021;48(8):611-623. doi: 10.1159/000518508. Epub 2021 Sep 21. PMID: 34569538; PMCID: PMC8619771.
- Kagan, K.O., Enders, M., Hoopmann, M., Geipel, A., Simonini, C., Berg, C., Gottschalk, I., Faschingbauer, F., Schneider, M.O., Ganzenmueller, T. and Hamprecht, K. (2021), Outcome of pregnancies with recent primary cytomegalovirus infection in first trimester treated with hyperimmunoglobulin: observational study. Ultrasound Obstet Gynecol, 57: 560-567. https://doi.org/10.1002/uog.23596
- Rawlinson WD, Boppana SB, Fowler KB, Kimberlin DW, Lazzarotto T, Alain S, Daly K, Doutré S, Gibson L, Giles ML, Greenlee J, Hamilton ST, Harrison GJ, Hui L, Jones CA, Palasanthiran P, Schleiss MR, Shand AW, van Zuylen WJ. Congenital cytomegalovirus infection in pregnancy and the neonate: consensus recommendations for prevention, diagnosis, and therapy. Lancet Infect Dis. 2017 Jun;17(6):e177-e188. doi: 10.1016/S1473-3099(17)30143-3. Epub 2017 Mar 11. PMID: 28291720.
- Iijima S. Pitfalls in the Serological Evaluation of Maternal Cytomegalovirus Infection as a Potential Cause of Fetal and Neonatal Involvements: A Narrative Literature Review. J Clin Med. 2022 Aug 26;11(17):5006. doi: 10.3390/jcm11175006. PMID: 36078936; PMCID: PMC9457027.
- Sarasini, A.; Arossa, A.; Zavattoni, M.; Fornara, C.; Lilleri, D.; Spinillo, A.; Baldanti, F.; Furione, M. Pitfalls in the serological diagnosis of primary human cytomegalovirus infection in pregnancy due to different kinetics of IgM clearance and IgG avidity index maturation. Diagnostics 2021, 11, 396.
- Kenji Tanimura, Shinya Tairaku, Ichiro Morioka, Kana Ozaki, Satoshi Nagamata, Mayumi Morizane, Masashi Deguchi, Yasuhiko Ebina, Toshio Minematsu, Hideto Yamada, Universal Screening With Use of Immunoglobulin G Avidity for Congenital Cytomegalovirus Infection, Clinical Infectious Diseases, Volume 65, Issue 10, 15 November 2017, Pages 1652–1658
- Tanimura K : Universal Screening With Use of Immunoglobulin G Avidity for Congenital Cytomegalovirus Infection. - Clinical infectious diseases : an official publication of the Infectious Diseases Society of America 2017;65(10):1652-1658
- Lazzarotto T, Guerra B, Lanari M, Gabrielli L, Landini MP. New advances in the diagnosis of congenital cytomegalovirus infection. J Clin Virol. 2008 Mar;41(3):192-7. doi: 10.1016/j.jcv.2007.10.015. Epub 2007 Dec 4. PMID: 18054840.
